生物医学工程相关
各种小问题
生物医学工程发展的战略原则:
1.医学应该努力使其目的适应经济 2.公正的和公平的医学 3.供得起的和可持续发展的医学
生物医学工程导论
生物医学工程的定义
生物医学工程是一门综合运用工程学、生物学和医学的理论与方法,在各层次上研究人体系统的状态变化,并运用工程技术手段去控制这类变化,以解决医学相关问题、保障人类健康的新兴交叉学科。
研究领域:生物材料、生物力学、医学成像与图像处理、生物医学信号处理、神经工程、组织工程、生物医学信息技术等
学科属性
1.高度交叉融合
- 工程学基础:以电子、机械、计算机、材料等传统工程学科为技术支撑。
- 医学与生物学内核:以人体生理、病理、解剖等医学知识及细胞、分子生物学为研究对象。
- 多学科渗透:还涉及物理学、化学、数学、信息科学等,形成“工程-医学-生物学”三位一体的知识体系。
2.应用导向性强
- 问题驱动:以临床医学和健康领域的实际需求(如疾病诊断、治疗、康复)为出发点。
- 技术转化:强调将工程技术转化为可用的医疗设备、系统或方法,直接服务于医疗实践。
3.研究层次跨度大
- 从微观的分子、细胞工程,到中观的组织、器官工程,再到宏观的人体系统乃至群体健康工程。
- 既包括机理探索,也涵盖产品研发与产业化。
4.创新性与前沿性
- 紧密跟随生物技术、信息技术、新材料等前沿科技发展,不断催生新的研究方向(如脑际接口、纳米医学、数字医疗等)。
- 是医疗健康领域技术创新的核心驱动力之一。
核心特征
以解决临床需求为根本导向,运用集成创新的工程方法,在跨越微观与宏观的多个层次上研究和干预生命系统,并始终受到伦理规范的严格约束。这使生物医学工程成为连接工程技术进步与人类健康福祉的关键桥梁。
发展历程
生物医学工程作为一门连接工程学与生命科学的交叉学科,其发展历程深刻反映了人类利用技术手段探索生命、对抗疾病的持续努力。其演进脉络可概括为四个主要阶段。
1.萌芽期:技术应用于医学的早期探索(19世纪-20世纪中期)
在此阶段,学科尚未正式建立,但物理学家和工程师已开始将工程技术原理应用于生理学和医学问题,相关研究分散于物理系、电子工程系和医学院的实验室中。
- 1895年:德国物理学家威廉·伦琴发现X射线,并迅速将其用于医学影像,成为工程物理技术直接服务于医学诊断的里程碑。
- 1903年:荷兰生理学家威廉·爱因托芬发明心电图机,将弦线电流计应用于记录心脏电活动,奠定了心血管工程诊断的基础。
- 20世纪20-50年代:人工肾(血液透析)原理被提出并初步实现,标志着工程学开始尝试替代人体器官功能;同时,科学家开始运用力学原理研究骨骼和血液流动,生物力学由此起源。
2.兴起与确立期:学科的独立与制度化(20世纪50年代-70年代)
二战后,科技的飞速发展为生物医学工程成为独立学科提供了土壤。
- 概念与组织诞生:“生物医学工程”一词最早在美国出现并得到正式使用。1958年,国际医学电子学联合会成立(1965年改称国际医学和生物工程联合会,后成为国际生物医学工程学会)。1968年,美国生物医学工程学会(BMES)成立。
- 学术建制化:20世纪50-60年代,美国约翰斯·霍普金斯大学、凯斯西储大学等高校率先成立了生物医学工程系或研究所,并设立专门的学位项目,这被视为学科独立的制度性标志。
- 关键里程碑:1958年,世界首例全埋藏式人工心脏起搏器成功植入,开启了植入式医疗设备的新纪元。
- 驱动力量:太空竞赛催生了小型化、可穿戴生物传感器的需求;固态电子技术革命(晶体管)使得医疗仪器得以便携化、复杂化;新材料发展(如高分子化学)推动了具有良好生物相容性植入器械的研发。此阶段核心领域集中在医学仪器、生物力学、人工器官和生物电信号处理。
3.快速发展期:技术爆炸与产业形成(约20世纪80年代起)
学科从单一设备研发转向多领域深度交叉,技术转化加速,产业规模迅速扩大。1984黏,美国生物医学工程和系统的市场规模已达到约110亿美元。
- 医学成像革命:1972年首台CT扫描机问世;1980年全身MRI进入临床,1984年获FDA认证,形成了“CT+MRI+PET”的现代医学影像诊断体系。
- 人工器官与生物材料:人工心脏瓣膜、人工肾(透析)、人工关节等实现规模化临床应用,硅橡胶、聚氨酯等生物材料成为核心载体。
- 介入医学工程:1977年首例冠状动脉球囊扩张术成功,结合数字减影血管造影(DSA)等技术,使微创介入诊疗成为常规手段。
4.成熟与扩展期:多学科深度融合与智能转型(21世纪至今)
学科边界持续拓宽,形成了从基础研究到产业转化的完整生态,并与人工智能、基因组学等前沿技术深度融合。
- 再生医学:诱导多功能干细胞(iPSCs)、类器官培养等技术为组织修复和器官移植带来新希望。
- 智能医疗:AI辅助诊断、手术机器人、可穿戴监护设备实现了疾病诊疗的精准化与实时化。
- 生物传感与芯片:微流控芯片、生物传感器推动了即时检测和个性化医疗发展。
- 神经工程崛起:脑机接口技术从实验室走向临床验证,为神经功能修复开辟了新途径。
- 纳米生物医学:利用纳米技术进行药物靶向输送和分子成像。
5.中国生物医学工程的发展
中国生物医学工程学科起步于20世纪70年代。著名医学家黄家驷院士是其最早的倡导者。1977年,中国协和医科大学创建了生物医学工程专业;1980年,中国生物医学工程学会成立,有力推动了学科发展。国内顶尖高校如清华大学(1979年设立)、东南大学(1984年由韦钰院士创立国内首个生物医学工程系)、华中科技大学(1981年成立生物医学工程系)等相继成为学科重镇。经过数十年发展,中国在该领域进步显著,自2019年以来,年发文量已跃居世界首位。
总结而言,生物医学工程从解决具体医疗器械需求的工程应用出发,逐步建立起独立的学科体系,经历了技术爆炸式的快速发展,最终演进为在分子、细胞、组织、器官和系统等多个尺度上进行精准干预和理解的综合性前沿学科,持续引领着医疗健康的未来。
国内发展现状:
国内生物医学工程发展现状呈现出规模快速扩张、创新活力迸发、政策强力驱动、但关键瓶颈仍存的鲜明特征,正从“跟跑”向“并跑”乃至部分领域“领跑”转变。
1.总体态势:进入高质量发展新阶段
中国已成为全球生物医学工程领域增长最快、最具活力的市场之一。学科与产业深度融合,基础研究(论文数量已居全球第一)与技术创新同步推进,在医学影像、高端植介入器械、体外诊断、智能医疗等细分领域实现了显著突破,国产化替代进程加速。
2.市场规模与增长动力
- 市场规模:2025年市场规模预计达1.2万亿人民币,占全球比重超15%,增速显著高于全球平均水平。
- 核心驱动力:国家资金和人才政策密集出台;人口老龄化和慢性病高发带来持续医疗需求;人工智能、基因编程、新材料等前沿技术与生物医学工程深度交叉融合,催生新业态。
3.政策环境:顶层设计强力支撑
国家《“十四五”生物经济发展规划》首次将生物经济提升至国家战略高度,明确将高端医疗器械、生物医用材料、医学人工智能等列为优先发展方向。监管改革深化,创新药械临床试验审评时限大幅缩短,并鼓励在海南自贸区等地开展细胞治疗、中药监管等改革试点。
4.前沿研究热点与创新方向
研究聚焦临床重大需求,呈现高度交叉融合态势。
- 生物医学大模型:专用AI模型处理海量生物医学数据,应用于辅助诊疗、药物研发。
- 侵入式脑机接口:如Neuralink的Blindsight技术,为神经功能修复提供新途径。
- 医疗机器人:手术、康复、护理机器人向智能化、微创化发展。
- 生物3D打印与再生医用材料:组织工程支架、可降解植入物需求激增,中国企业在相关材料领域掌握全球约17%的核心专利。
- 基因编辑与细胞治疗:CAR-T、干细胞治疗等新技术加速临床转化。
此外,可穿戴闭环感知设备、医学影像AI、数字疗法、类器官与数字孪生等也是当前研究前沿。
5.产业发展现状
细分领域格局:医学影像设备、体外诊断(IVD)、高值医用耗材、康复器械构成四大核心板块,合计占市场规模的76.4%。其中,国产CT、MRI等高端设备市场占比持续提升。
代表企业崛起:联影医疗、东软医疗在高端影像设备领域突破;迈瑞医疗在生命信息与支持领域领先;华大基因、达安基因在基因测序和分子诊断方面具备全球影响力。
资本高度活跃:2024年行业一级市场融资总额达528亿元,超60%资金流向智能可穿戴、神经接口、组织工程等前沿创新企业。
6.主要挑战与瓶颈
成果转化低:科技成果转化率仅5%左右,远低于发达国家(25%-30%)。制度障碍(如国有资产评估耗时)、早期概念验证资金短缺是核心瓶颈。
关键核心技术受制于人:高端生物反应器、色谱填料、特种生物材料等核心试剂、耗材与设备仍高度依赖进口。
原始创新能力待加强:全球首创新药(First-in-class)占比低,底层技术积累仍需时日。
复合型人才缺口巨大:兼具工程、医学、生物学背景的跨界人才,以及技术转移专业人才严重短缺。
7.未来展望
在“健康中国2030”战略指引下,中国生物医学工程正朝着智能化、精准化、普惠化、全球化方向加速演进。未来竞争的关键在于:突破底层核心技术、构建高效的“产学研医金”协同转化生态、培养高端复合型人才,并深度参与全球创新合作与竞争,最终实现从产业大国向产业强国的跨越。
核心研究范畴
生物医学工程的核心研究范畴与学科分支体现了其高度交叉融合的本质。其研究旨在从分子、细胞、组织、器官到系统等多个尺度上,运用工程学原理与方法,解决医学诊断、治疗、康复和健康促进中的关键问题。不同高校和研究机构根据自身优势形成了各有侧重的方向体系。
一、核心研究范畴(按技术领域划分)
生物医学工程的研究主要围绕以下几个核心范畴展开:
1.生物力学与生物材料
生物力学:运用力学原理研究生物体(如骨骼、心血管、软组织)的力学特性、运动规律及其与功能的关系,为人工器官设计、疾病机理研究和康复工程提供理论基础。
生物材料:研发能与人体组织相容并执行特定功能(如替代、修复、药物递送)的材料,如人造关节、血管支架、组织工程支架等。
2.生物医学电子、仪器与传感
生物医学电子与医疗仪器:面向临床需求,开展生理信息(心电、脑电等)检测与处理、远程医疗、健康监护,并设计开发新型医疗仪器与设备。
生物传感器:研发用于疾病早期筛查、慢性病动态监测的高灵敏度、高特异性、便携化传感装置。
3.医学影像与信息学
医学影像:致力于开发与优化各种医学成像技术(如CT、MRI、超声、核医学),提高疾病诊断的准确性与效率。
医疗人工智能与信息学:利用人工智能、大数据技术处理医学影像、临床数据,开发疾病诊断模型与临床决策支持系统,推动精准医疗。
4.组织工程与再生医学
旨在修复或再生受损的组织和器官。通过结合生物材料、细胞(如干细胞)和生长因子,在实验室构建人工皮肤、软骨等,或开发刺激体内组织再生的策略。
5.生物信息学与计算生物学
利用计算机科学和信息技术,对海量生物医学数据(如基因组、蛋白质组数据)进行获取、存储、分析和挖掘,以揭示生命规律、辅助疾病研究和药物设计。
6.神经工程
研究神经系统功能,开发用于治疗神经系统疾病或实现脑机交互的设备与技术,如人工耳蜗、深部脑刺激器、脑机接口等。
7.纳米生物医学与分子工程
在微观层面应用工程原理,研究纳米材料在药物靶向输送、分子成像、疾病早期诊断等方面的应用。
主要学科分支表:
| 分支方向 | 核心研究内容 | 典型应用与产出 |
|---|---|---|
| 生物医学成像 | 医学影像设备研发、图像重建与处理算法、多模态成像融合。 | 新型CT/MRI系统、AI辅助诊断软件、分子影像探针。 |
| 生物材料 | 医用材料的合成、改性、生物相容性评价、表面功能化。 | 人工骨、心脏瓣膜、可降解血管支架、药物缓释载体。 |
| 组织工程与再生医学 | 细胞-材料相互作用、生物反应器、干细胞定向分化、类器官构建。 | 人工皮肤、软骨修复支架、生物3D打印器官雏形。 |
| 生物信息学与计算生物学 | 基因组/蛋白质组数据分析、生物网络建模、疾病预测算法。 | 癌症基因分型、新药靶点发现、个性化治疗方案。 |
| 神经工程 | 神经信号解码与编码、神经接口器件、神经调控技术与康复。 | 脑机接口、人工视网膜/耳蜗、帕金森病脑深部电刺激。 |
| 医疗器械与仪器 | 医疗设备软硬件设计、系统集成、可靠性验证、人机交互。 | 便携式监护仪、手术机器人、可穿戴健康设备、体外诊断仪器。 |
| 生物力学与机械生物学 | 细胞与组织对外力刺激的响应机制、运动生物力学、仿生设计。 | 个性化假肢与矫形器、心血管支架优化、运动损伤防护。 |
| 细胞与生物分子工程 | 细胞代谢工程、合成生物学、基因编辑工具开发、生物催化。 | 工程化细胞疗法、新型疫苗平台、生物制造。 |
| 药物与基因递送系统 | 纳米载体设计、靶向递送策略、控释技术、基因编辑工具递送。 | 靶向抗癌纳米药物、mRNA疫苗递送系统、基因治疗载体。 |
| 专业方向编号 | 专业方向 | 指导教师 |
|---|---|---|
| 01 | 医学超声 | 林浩铭,陈昕,胡亚欣,沈圆圆,陆敏华 |
| 02 | 医学图像与信息处理 | 余夏夏,王毅,汪天富,薛武峰,高毅,牟天,蒋宇超,蔡嘉月,刁现芬,刘忠,张力,杨鹏,岳广辉,雷柏英,黄炳升,程君,梁臻,黄若冰,黄淦,杜杰 |
| 03 | 体外诊断技术及仪器 | 张雅各,孔湉湉,李自达,陈雯雯,孔彬,徐海华,柴语鹃 |
| 04 | 医疗电子技术及应用 | 周永进,张旭,但果,丁惠君,彭珏,于妍妍 |
| 05 | 生物传感与成像 | 许改霞,杨成彬,高壮强,徐周睿 |
伦理、安全与监管
生物医学工程的伦理、安全与监管构成了保障其健康发展的三大支柱。伦理是价值导向,确保技术发展不偏离“以人为本”的宗旨;安全是技术底线,通过系统性风险管理确保产品与研究的可靠性;监管是制度保障,通过法律法规和标准强制各方遵守规则。三者相互关联,共同约束和引导着这一深刻影响人类生命健康的领域。
生物医学工程的伦理、安全与监管共同构成了一个动态发展的治理生态系统。当前面临的挑战包括:技术超前性与伦理/监管滞后性的矛盾(如脑机接口的数据隐私)、全球科技伦理共识的构建(如基因编辑的全球治理)、以及高昂技术成本与普惠医疗之间的张力。
生物医学基础
医学基础
心血管系统
心血管系统,又称循环系统,是人体的“生命运输线”,其核心功能是通过血液的持续循环,实现物质运输、内环境稳态调节和免疫防御。
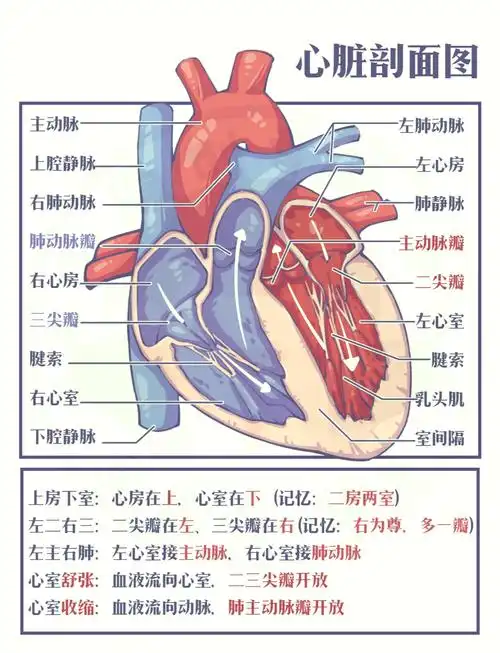
一、解剖结构与其功能角色:
| 结构组成 | 解剖特点 | 功能角色 |
|---|---|---|
| 心脏 | 中空的肌性器官,分为左、右心房和心室,瓣膜确保单向血流。 | 动力泵:通过节律性收缩(射血)与舒张(充盈),为血液流动提供原动力。左心泵血至全身(体循环),右心泵血至肺部(肺循环)。 |
| 血管 | 动脉:管壁厚、弹性好,承受高压。 毛细血管:管壁极薄,仅单层内皮细胞,分支成网。 静脉:管壁较薄、容量大,有静脉瓣防止血液逆流。 | 运输与分配网络:动脉将血液输送到组织;毛细血管是物质交换的场所;静脉将血液回流至心脏。 |
| 血液 | 由血浆(水分、蛋白质、电解质等)和血细胞(红细胞、白细胞、血小板)组成。 | 运输载体与防御介质:是溶解和承载各种物质的液体,同时包含免疫和凝血成分。 |
二、生理功能
1.运输功能:物质的长途配送与垃圾清运
氧气与二氧化碳的运输:
- 肺循环(右心-肺-左心):右心室将含氧量低的静脉血泵入肺动脉,在肺部毛细血管,红细胞中的血红蛋白释放二氧化碳并结合氧气,变为动脉血,经肺静脉回左心房。
- 体循环(左心-全身-右心):左心室将富氧的动脉血泵入主动脉,输送到全身各器官组织的毛细血管网。在这里,氧气和营养物质从血液扩散到组织细胞,同时组织细胞代谢产生的二氧化碳和废物进入血液,血液变为静脉血,经上下腔静脉回右心房。
营养与废物的运输:将从消化道吸收的营养物质(葡萄糖、氨基酸、脂类)运至全身;将细胞代谢产生的废物(如尿素、肌酐)运至肾脏、皮肤等排泄器官。
激素的运输:作为体液调节的主要途径,将内分泌腺分泌的激素(如胰岛素、肾上腺素)精准、快速地运送到靶器官,实现远距离调节。
2.调节功能:维持内环境稳态
心血管系统本身是稳态的核心,也参与全身的调节。
血压调节:通过神经调节(如压力感受器反射)和体液调节(如肾素-血管紧张素系统),实时调整心输出量和外周血管阻力,维持稳定的血压,保证各器官的血液灌注。
血流分布调节:根据器官需求动态分配血流。例如,运动时,通过调节血管舒缩,使骨骼肌血流量大幅增加,而消化器官血流量相对减少。
体温调节:皮肤毛细血管的舒缩是调节散热的关键。体温升高时,皮肤血管扩张,血流量增加,散热增多;反之则减少散热。
3.保护功能:免疫与防御
免疫与防御:白细胞(如中性粒细胞、淋巴细胞)通过血液循环巡逻全身,可迅速迁移到感染或损伤部位,执行吞噬、产生抗体等免疫功能。
凝血与止血:当血管损伤时,血小板在局部粘附、聚集,并启动凝血cascade,形成血凝块,有效防止失血。这一过程也依赖于血液的正常循环。
三、功能实现的整合:一个精密的闭环工程
心血管系统的功能并非由各个部件独立完成,而是一个高度整合的闭环反馈系统:
1.需求感知:组织代谢活跃(如运动)导致氧含量下降、二氧化碳和代谢产物增加,这些化学变化被局部感受器感知。
2.指令下达与执行:信息通过神经和体液途径传至心脏和血管。心脏增加心率和心肌收缩力以提高心输出量;局部血管(如运动肌肉的动脉)扩张以增加血流量。
3.物质高效交换:增多的血流流经扩张的毛细血管,在静水压和渗透压的共同作用下,加速与组织液进行物质交换。
4.回流与再循环:交换后的静脉血通过静脉系统(借助肌肉泵、呼吸泵等机制)克服重力回流至心脏,完成循环。
总结:心血管系统的核心功能时一个以心脏为泵、血管为路、血液为车的、永不停歇的精密物流与管理系统。它确保了生命活动所需物质的即时供应与废物的即时清除,并深度参与机体调节与防御,是维持生命稳态的基石。任何结构或功能的异常(如心瓣膜损坏、动脉硬化、心力衰竭)都会导致整个系统效率下降,引发一系列疾病。
呼吸系统
呼吸系统的核心功能是实现机体与外界环境之间的气体交换,即吸入氧气(
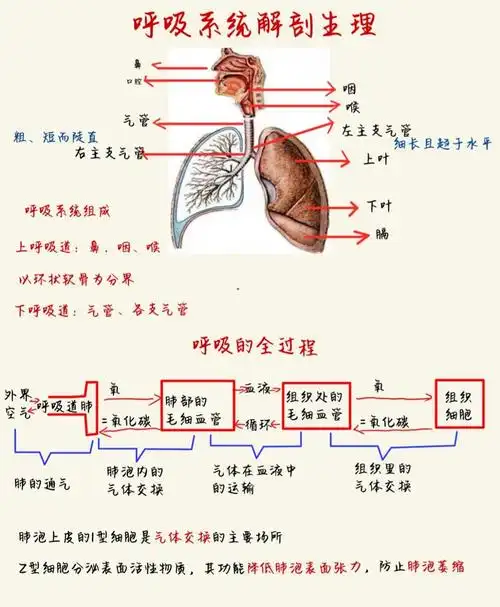
一、解剖结构与其功能角色
| 结构组成 | 解剖分区与特点 | 功能角色 |
|---|---|---|
| 传导性气道(呼吸道) | 上呼吸道:鼻、咽、喉。鼻黏膜富含血管和腺体,可加温、加湿、过滤空气。 下呼吸道:气管、支气管、细支气管。管壁有软骨环支撑,防止塌陷;黏膜有纤毛和杯状细胞。 | 气体通道与预处理:为空气进出肺提供通道,并对其进行过滤、加温、加湿和清洁。 |
| 呼吸性区域(气体交换场所) | 呼吸性细支气管、肺泡管、肺泡囊和肺泡。肺泡是半球形囊泡,壁极薄,由单层肺泡上皮细胞和丰富的毛细血管网包绕。 | 气体交换的场所:肺泡是O₂和CO₂通过扩散进行交换的唯一部位。巨大的表面积(成人约70-100㎡)和极短的气-血距离(<0.5µm)确保了高效交换。 |
| 肺与胸廓 | 肺:左二右三叶,富有弹性,位于胸腔内。 胸廓:由肋骨、胸骨、脊柱和肌肉构成。 胸膜腔:脏层与壁层胸膜之间的潜在腔隙,内有少量浆液。 | 动力与容器:胸廓是呼吸运动的“风箱”,肺是弹性“气囊”。胸膜腔的负压将两者耦联,使肺能随胸廓运动而扩张和回缩。 |
| 呼吸肌 | 主要吸气肌:膈肌(最重要)、肋间外肌。 辅助吸气肌:斜角肌、胸锁乳突肌等。 呼气肌:肋间内肌、腹肌(平静呼气是被动的)。 | 呼吸动力源:通过收缩与舒张改变胸廓容积,产生肺通气的压力差。 |
二、生理功能:气体交换
1.肺通气:气体进出肺的过程
- 原理:基于压力差。呼吸肌收缩使胸廓扩大 --> 胸膜腔内负压增大 --> 肺被动扩张 --> 肺内压暂时低于大气压 --> 空气流入(吸气);呼吸肌舒张 --> 胸廓和肺弹性回缩 --> 肺内压高于大气压 --> 气体流出(呼气)
- 关键指标:潮气量(每次平静呼吸吸入或呼出的气量)、肺活量(最大吸气后尽力呼出的气量,反映通气储备能力)。
2.肺换气:肺泡与血液之间的气体交换
- 原理:基于气体分压差和扩散。肺泡内
分压高, 分压低;流经肺泡毛细血管的静脉血中 分压低, 分压高。因此, 从肺泡扩散入血, 从血扩散入肺泡。 - 影响因素:气体扩散速率受分压差、气体溶解度、扩散面积(肺泡总面积)和扩散距离(呼吸膜厚度)影响。肺水肿、肺纤维化等疾病回增厚呼吸膜,严重损害换气功能。
3.气体在血液中的运输
氧气运输:
- 物理溶解(1.5%):直接溶解于血浆。
- 化学结合(98.5%):与红细胞内的血红蛋白(
)结合形成氧合血红蛋白( )。这是高效运输的关键。
二氧化碳运输:
- 物理溶解(5%)。
- 化学结合(95%):主要以碳酸氢盐(
)形式(在血浆中,约占70%),以及与血红蛋白结合形成氨基甲酰血红蛋白(在红细胞内约占23%)的形式运输。 的运输过程对血液酸碱平衡有重要调节作用。
4.组织换气:血液与组织细胞之间的气体交换
- 原理:同样基于分压差的扩散。在组织毛细血管中,由于细胞代谢不断消耗
、产生 ,因此组织液中 分压低于动脉血, 分压高于动脉血。于是, 从血液扩散入组织细胞, 则从组织细胞扩散入血液。
三、功能的整合与高级调节
1.呼吸中枢的节律性控制:延髓和脑桥的呼吸中枢产生基本的呼吸节律,并通过神经(膈神经、肋间神经)支配呼吸肌。
2.化学感受性反射(核心调节机制):
- 中枢化学感受器(位于延髓腹外侧):主要感受脑脊液中
分压升高引起的 浓度变化,是调节呼吸的最强刺激。 - 外周化学感受器(颈动脉体和主动脉体):主要感受动脉血
分压显著降低,也感受 分压升高和 浓度升高。 - 调节过程:当血中
升高(或 显著降低、 升高) --> 刺激化学感受器 --> 呼吸中枢兴奋 --> 呼吸加深加快 --> 排出更多 ,吸入更多 --> 恢复血液气体正常水平
总结:
呼吸系统是一个由传到气道、肺泡、胸廓和呼吸肌构成的精密“气体交换站”。其核心功能是通过通气、换气、运输和组织换气四个连续环节,高效完成氧气的摄入和二氧化碳的排出。这一过程不仅维持了细胞代谢所需,还深度参与内环境酸碱平衡的调节,并受神经和化学因素的精密反馈控制。它与心血管系统紧密耦联(心肺一体),共同保障了生命活动的能量供应和代谢废物的清除。
神经系统
神经系统是人体最复杂、最精密的调控系统,其核心功能可概括为:接收、整合、传递信息,并以此精确调控机体的所有活动,以适应内外环境变化,维持生命稳态。
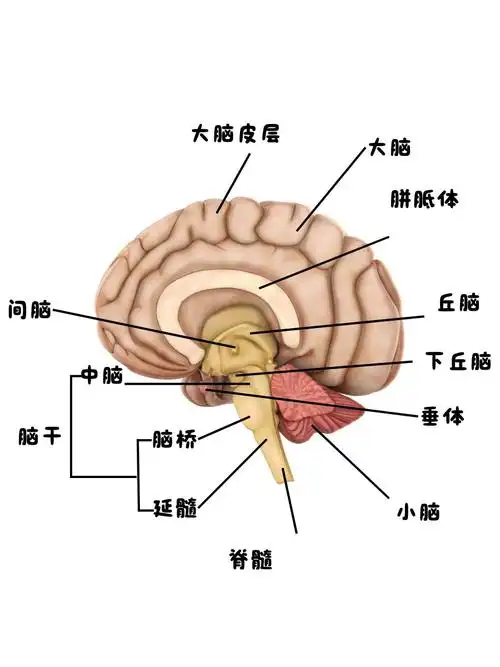
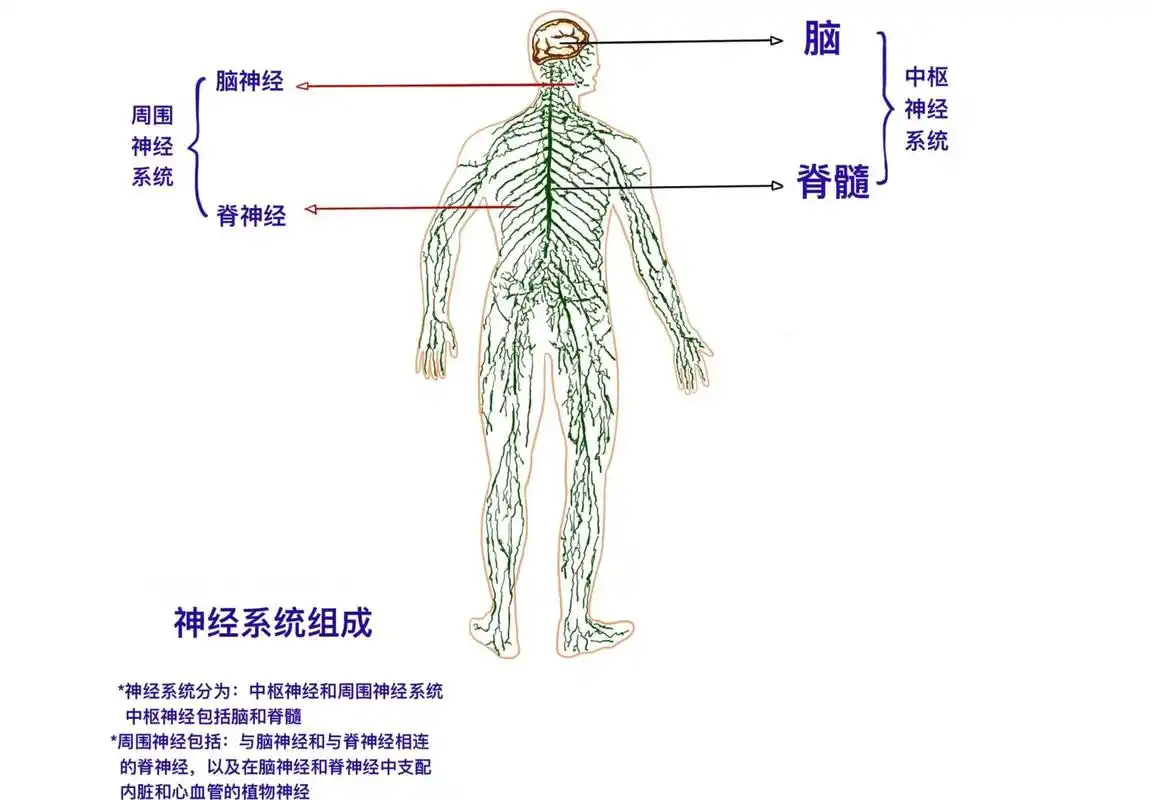
一、核心解剖结构与其功能角色
神经系统从解剖上可分为中枢神经系统和周围神经系统两大部分,它们共同构成一个完整的“指挥-通信”网络。
| 结构大类 | 主要组成部分 | 解剖特点与核心功能角色 |
|---|---|---|
| 中枢神经系统 (CNS) 指挥中心 | 脑 | 最高级整合与决策中枢。分为: • 端脑(大脑):表面为大脑皮层,按功能分为额叶(运动、决策、个性)、顶叶(躯体感觉、空间定位)、颞叶(听觉、语言理解、记忆)、枕叶(视觉处理)。内部有基底核(调节运动)、边缘系统(含海马体与杏仁核,调控情绪与记忆)。 • 间脑:含丘脑(几乎所有感觉信息上传至皮层的中继站)和下丘脑(调节体温、摄食、内分泌、昼夜节律等内稳态的“总开关”)。 • 小脑:位于后颅窝,协调随意运动、维持身体平衡、调节肌张力。 • 脑干(延髓、脑桥、中脑):生命中枢,调控呼吸、心跳、血压等基本生命活动,是上下行神经纤维的必经通道,包含多数颅神经核。 |
| 脊髓 | 信息传导通道与低级反射中枢。位于椎管内,内部为“H”形灰质(含运动、感觉神经元胞体),外部为白质(上下行神经纤维束)。负责传递脑与身体之间的信息,并能独立完成膝跳反射、排尿反射等简单反射。 | |
| 周围神经系统 (PNS) 通信网络 | 躯体神经系统 | 受意识支配。包括: • 脑神经(12对):主要支配头面部的感觉和运动。 • 脊神经(31对):支配躯干和四肢的感觉与运动。 其传出纤维支配骨骼肌,产生随意运动;传入纤维将皮肤、肌肉的感觉信息传至中枢。 |
| 自主神经系统 (植物神经系统) | 不受意识直接控制,支配心肌、平滑肌和腺体,调节内脏活动。分为功能相互拮抗的两部分: • 交感神经:“战斗或逃跑”系统,在应激、紧张时激活,使心跳加快、血压升高、瞳孔扩大。 • 副交感神经:“休息与消化”系统,在安静状态下活跃,促进消化、降低心率、保存能量。 两者共同维持内环境(如心率、消化、腺体分泌)的动态平衡。 |
二、生理功能:信息处理与高级调控
神经系统的功能围绕信息的输入、整合、输出这一核心流程展开,并在此基础上衍生出复杂的高级功能。
1.感受功能:信息的接收与输入
- 原理:遍布全身的感受器(如皮肤中的痛温觉感受器、视网膜的感光细胞)接收内外环境刺激,并将其转化为电信号(神经冲动)。
- 通路:信号由感觉神经元(传入神经元)通过周围神经(脊神经、脑神经)传入脊髓和脑干,最终经丘脑中继后投射到大脑皮层的特定感觉区(如中央后回的躯体感觉皮层)进行感知。
2.整合功能:信息的分析与决策
- 分析与处理:大脑皮层(特别是联合区)对传入的感觉信息进行综合、分析、比较和解释,形成知觉,并与存储的记忆进行关联。
- 决策与规划:前额叶皮层等高级中枢根据整合后的信息,指定行为计划、做出决策、解决问题。
- 记忆与学习:海马体是形成新记忆的关键结构,它负责将短期记忆巩固为长期记忆,存储与大脑皮层的广泛区域。
3.运动功能:指令的执行与输出
- 原理:整合后的决策转化为运动指令。
- 通路:指令从大脑皮层的初级运动皮层发出,经锥体束下行至脊髓,再由脊髓的运动神经元传出,支配骨骼肌收缩,产生精确的随意运动。
- 协调与修正:小闹在运动执行过程中,实时接收来自大脑皮层和身体感觉的反馈,精细调节运动的时机、力度和协调性,确保动作流畅准确。基底核则参与运动的起始、终止和模式选择。
4.高级认知与稳态调节
- 语言:布罗卡区(额叶)负责语言表达,韦尼克区(颞叶)负责语言理解,两者协同完成复杂的语言功能。
- 情绪与行为:边缘系统(特别是杏仁核)是情绪处理的中心,调控恐惧、愉悦等基本情绪反应,并与前额叶皮层联系,影响决策和社会行为。
- 维持内稳态:下丘脑是神经-内分泌系统的整合中心,通过调节激素释放和自主神经活动,精确控制体温、摄食、水盐平衡和昼夜节律。脑干的延髓直接控制呼吸、心跳等生命体征。
三、功能实现的细胞与分子基础
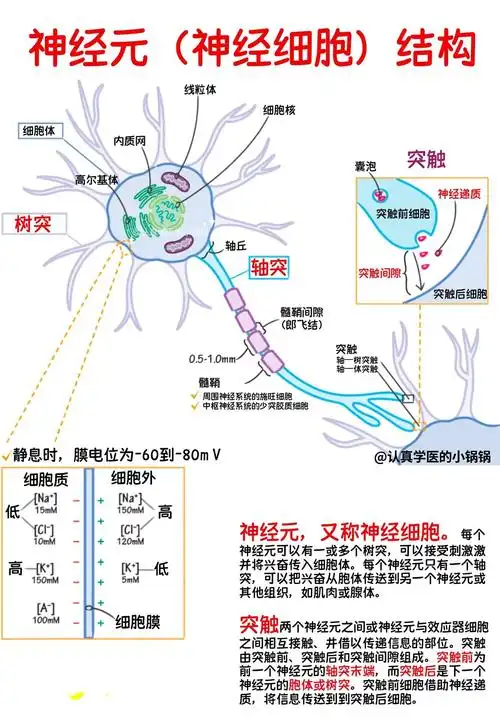
1.基本单位:神经元
- 结构:由胞体(整合信号)、树突(接收信号)和轴突(传导信号)构成。
- 工作原理:通过动作电位(一种由
离子通道开闭产生的电信号)沿轴突传导信息。在突触处,电信号转化为化学信号--释放神经递质(如乙酰胆碱、多巴胺、谷氨酸),作用于下一神经元,完成信息传递。
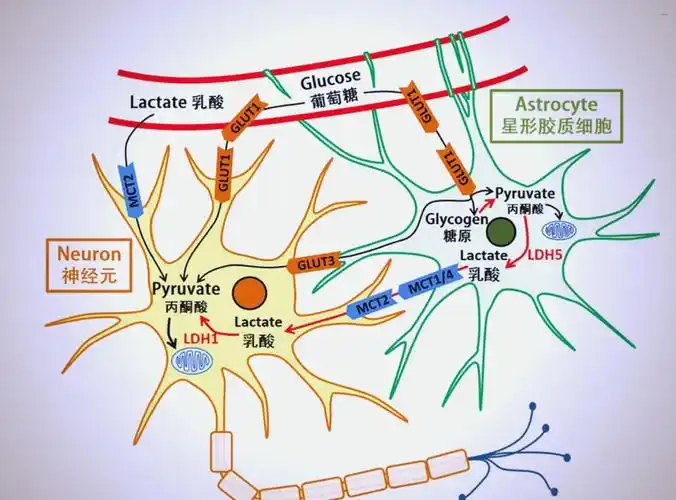
2.支持系统:神经胶质细胞
- 数量远多于神经元,不直接传导冲动,但对神经元功能至关重要。
- 少突胶质细胞(CNS)和施万细胞(PNS)形成髓鞘,包裹轴突,实现跳跃式传导,极大提高信号传导速度。
- 星形胶质细胞:构成血脑屏障,选择性控制物质进出脑组织,维持神经元微环境稳定,并提供营养支持。
- 小胶质细胞:作为中枢神经系统的免疫细胞,负责监视、清除损伤或感染的细胞。
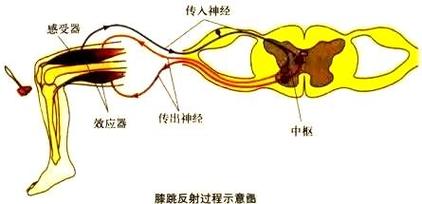
四、功能的整合:反射与可塑性
- 反射弧:是神经系统功能活动的基本方式,体现了其快速反应能力。由感受器、传入神经、反射中枢、传出神经和效应器
- 神经可塑性:指神经系统结构和功能在经验、学习或损伤后发生适应性改变的能力。这是学习、记忆以及中风后功能康复的生物学基础。
总结:
神经系统是一个以中枢为指挥塔、周围为通信网、神经元为信使的超级信息处理系统。它通过感觉、整合、运动三大核心流程,不仅维持着呼吸、心跳等基本生命活动,更孕育了思维、语言、情感等人类独有的高级智慧。其功能的实现,依赖于从宏观脑区到微观离子通道的每一级结构的精密协作,是生物学中最具魅力的复杂系统之一。
消化系统
消化系统的核心功能是将摄入的食物转化为可被机体吸收的小分子营养物质,并排出未被吸收的残渣。这一过程涉及复杂的物理型粉碎、化学性分解、选择性吸收和废物成形。
消化系统的核心功能是将摄入的食物转化为可被机体吸收利用的小分子营养物质,并排出未被吸收的残渣。这一过程涉及复杂的物理性粉碎、化学性分解、选择性吸收和废物成形,是一个高度协调的连续生理过程。
一、解剖结构与其功能角色
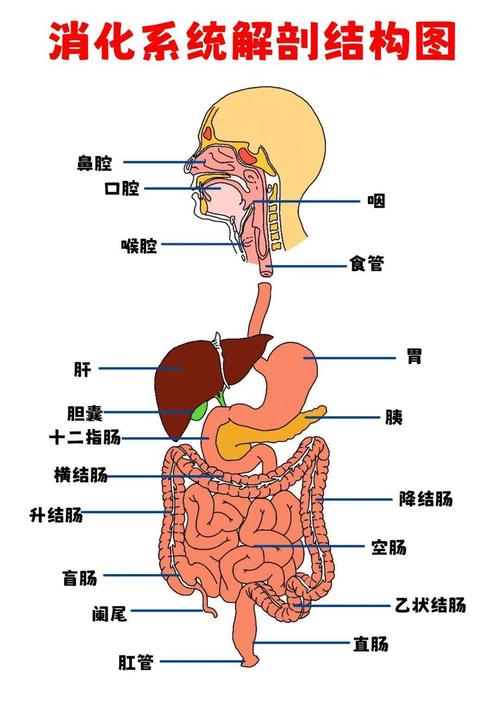
消化系统由消化管和消化腺两大部分组成,形成一条从口到肛门的连续管道及附属器官。
| 结构类别 | 主要组成部分 | 解剖特点与核心功能角色 |
|---|---|---|
| 消化管 (食物通道与加工厂) | 口腔 | 摄入与初步加工。含牙齿(机械咀嚼)、舌(搅拌、味觉、吞咽)、唾液腺开口。是机械消化(咀嚼)和化学消化(唾液淀粉酶分解淀粉)的起始点。 |
| 咽与食管 | 输送通道。咽是呼吸与消化的交叉路口,吞咽时关闭呼吸道;食管是肌性管道,通过蠕动将食团推送入胃。 | |
| 胃 | 储存、混合与初步消化。J形囊状器官,胃壁有纵行、环行和斜行三层平滑肌。功能:1. 暂时储存食物;2. 机械性消化(通过蠕动将食物与胃液混合成食糜);3. 化学性消化(胃蛋白酶原在酸性环境下激活为胃蛋白酶,开始蛋白质消化);4. 分泌内因子(助维生素B₁₂吸收)。 | |
| 小肠 | 消化与吸收的核心场所。分为十二指肠、空肠、回肠。其黏膜层形成环状皱襞、绒毛和微绒毛,使吸收表面积增加约600倍。功能:1. 完成化学消化(胰液、胆汁、小肠液在此作用);2. 吸收绝大部分营养物质(糖、氨基酸、脂肪酸、维生素、矿物质、水)。 | |
| 大肠 | 水分吸收与废物成形。分为盲肠、结肠(升、横、降、乙状)、直肠。功能:1. 吸收水分和电解质,将液态食糜转化为半固体粪便;2. 储存粪便;3. 肠道菌群发酵未消化的膳食纤维,产生短链脂肪酸和维生素K等。 | |
| 消化腺 (化学消化液工厂) | 唾液腺(腮腺、颌下腺、舌下腺) | 分泌唾液,含唾液淀粉酶和黏液,润滑食物并开始淀粉消化。 |
| 肝 | 最大的消化腺和代谢中心。功能:1. 分泌胆汁(储存于胆囊),胆汁中的胆盐乳化脂肪,增大与脂肪酶的接触面积;2. 代谢营养物质(糖原合成与分解、脂肪代谢、蛋白质合成);3. 解毒。 | |
| 胰 | 最重要的消化液分泌器官。分泌胰液,经胰管排入十二指肠。胰液含胰淀粉酶、胰脂肪酶、胰蛋白酶原/糜蛋白酶原等,能彻底消化碳水化合物、脂肪和蛋白质。同时,胰岛分泌胰岛素和胰高血糖素,调节血糖。 | |
| 胃腺、肠腺 | 分别分泌胃液和小肠液,参与局部化学消化。 |
二、生理功能:消化与吸收
1.摄入与初步加工(口腔)
- 机械消化:牙齿咀嚼将大块食物磨碎,增加其表面积。
- 化学消化:唾液中的唾液淀粉酶将部分淀粉分解为麦芽糖。
- 形成食团:舌将食物与唾液混合,形成易于吞咽的食团。
2.转运与胃内处理(咽、食管、胃)
- 吞咽:是一个复杂的反射过程,确保食团进入食管而非气管。
- 胃的运动与分泌:
- 容受性舒张:胃上部肌肉舒张,接纳食物,避免压力骤升。
- 蠕动:胃中部和下部肌肉节律性收缩,将食物与胃液(含盐酸、胃蛋白酶原、黏液)混合成半流体的食糜。
- 盐酸:激活胃蛋白酶原为胃蛋白酶(分解蛋白质),并提供酸性杀菌环境。
- 排空:胃窦蠕动将食糜分批推入十二指肠,排空速度受食糜成分(脂肪最慢)和十二指肠反馈调节。
3.核心消化与吸收(小肠)
化学消化的完成:
- 胰液(碱性):中和来自胃的酸性食糜,并提供最全面的消化酶(胰淀粉酶、胰脂肪酶、胰蛋白酶、糜蛋白酶等),完成对三大营养物质的最终分解。
- 胆汁:不含酶,但其中的胆盐能将脂肪乳化为微滴,极大促进脂肪酶的作用。
- 小肠液:含多种消化酶,进行最后的“精加工”。
吸收的主要部位:
- 糖类:被分解为单糖(葡萄糖、半乳糖、果糖)后,主要通过小肠上皮细胞的主动转运和易化扩散吸收入血。
- 蛋白质:被分解为氨基酸和小肽后,主要通过主动转运吸收入血。
- 脂肪:被分解为脂肪酸、甘油一酯后,与胆盐形成混合微胶粒,扩散入上皮细胞。在细胞内重新合成甘油三酯,与载脂蛋白结合形成乳糜微粒,进入淋巴循环,最终汇入血液循环。
- 水、维生素、矿物质:主要通过被动扩散或主动转运吸收。
4.浓缩与排泄(大肠)
- 吸收:主要吸收水分和电解质(
),每日可吸收约1.5升水。 - 菌群作用:结肠内大量共生细菌发酵未被消化的膳食纤维,产生气体(如氢气、甲烷)和有益的短链脂肪酸(如丁酸),后者可为结肠细胞供能。
- 粪便形成与排便:残渣、细菌、脱落细胞等形成粪便,储存于乙状结肠和直肠。当直肠内压达到阈值时,引发排便反射(受意识高级中枢调控)。
三、功能的整合与调节
消化系统的活动受到精密的神经调节和体液(激素)调节,确保其与机体的整体状态相适应。
1.神经调节:
- 外来神经:副交感神经(迷走神经为主)兴奋时,促进消化腺分泌和胃肠运动;交感神经兴奋时,抑制消化活动(备战状态)。
- 内在神经:肠神经系统(ENS),被称为“第二大脑”,能相对独立地调节局部消化活动,如协调小肠的分节运动(混合食糜)和蠕动(推进食糜)。
2.体液调节(胃肠激素):
- 促胃液素:由胃窦G细胞分泌,刺激胃酸和胃蛋白酶分泌。
- 缩胆囊素:由小肠I细胞分泌,刺激胆囊收缩排出胆汁,刺激胰酶分泌。
- 促胰液素:由小肠S细胞分泌,刺激胰液(富含
)大量分泌以中和胃酸。 - 这些激素根据食糜的成分和量,被精确释放,形成完美的反馈调节环路。
总结:
消化系统是一个设计精妙的生物化工厂与物流系统。消化管是贯穿始终的生产线和运输线,而消化腺则是提供关键化学试剂的附属车间。其核心功能通过机械消化与化学消化相结合、消化与吸收相衔接、神经与激素调节相协同的方式得以完美实现。整个过程始于口腔的主动摄入,终于大肠的废物排出,其中小肠是绝对的“核心车间”,承担了终末消化和绝大部分吸收的重任。这一系统的高效运作,为机体的生长、修复和所有生命活动提供了必需的物质和能量基础。
生物学基础
细胞结构
细胞的基本结构框架:膜、质、核
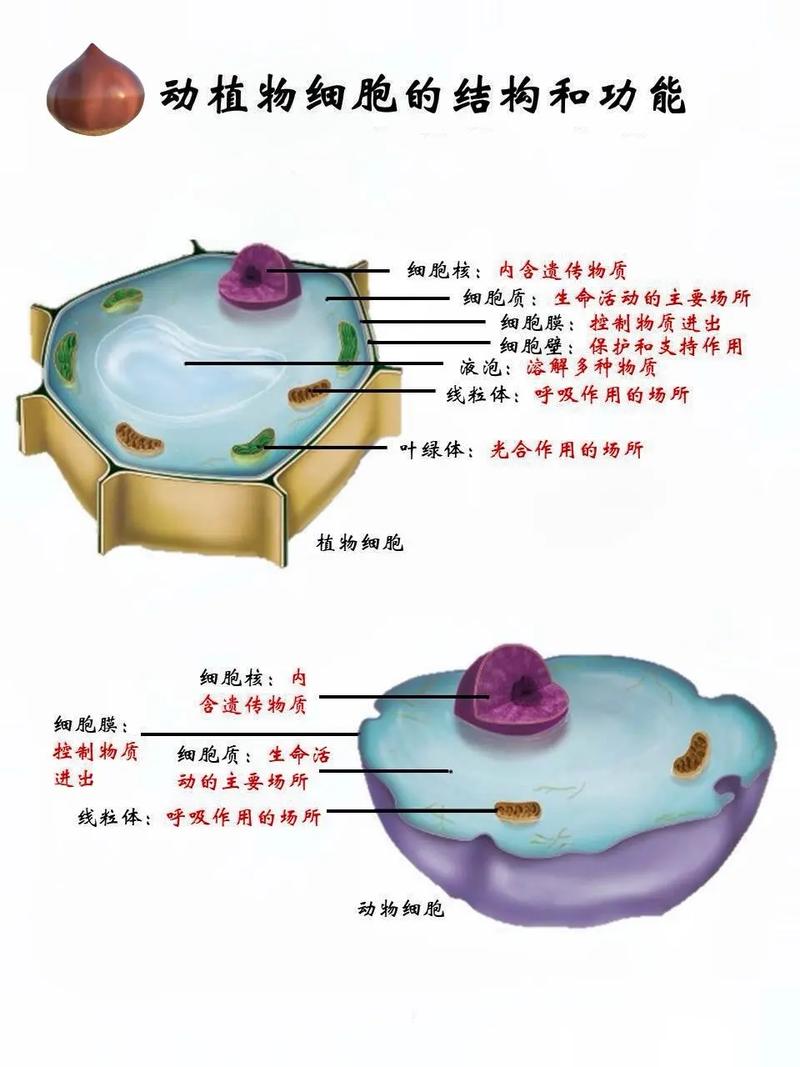
中心法则
中心法则是分子生物学中描述遗传信息在细胞内传递方向与规律的核心框架。它阐明了遗传信息从DNA到RNA,再到蛋白质的序列流动,是理解生命运作分子逻辑的基石。
经典的中心法则定义了信息传递的三个核心步骤和不可逆的方向性。
信息流动的主干道:DNA → RNA → 蛋白质
1.复制:以亲代DNA为模板,合成子代DNA的过程。
- 目的:在细胞分裂前,实现遗传信息的完整、精确拷贝,保证遗传的稳定性。
- 关键分子:DNA聚合酶等复制复合体。
- 模板与产物:模板是DNA双链,产物是两条相同的DNA双链(半保留复制)。
2.转录:以DNA的一条链为模板,合成一条互补RNA链的过程。
- 目的:将储存在DNA中的遗传信息“抄录”成RNA版本,以便离开细胞核并指导蛋白质合成。
- 关键分子:RNA聚合酶。
- 模板与产物:模板是DNA的模板链,产物是单链RNA(如mRNA、rRNA、tRNA)。
3.翻译:以mRNA的碱基序列为指令,合成具有特定氨基酸序列的多肽链(蛋白质)的过程。
- 目的:将核酸语言(碱基序列)转换为蛋白质语言(氨基酸序列),实现遗传信息的最终表达。
- 关键分子:核糖体(由rRNA和蛋白质构成)、tRNA(携带特定氨基酸并识别密码子)。
- 模板与产物:模板是mRNA,产物是多肽链。
| 过程 | 主要模板 | 主要产物 | 关键酶/复合体 | 发生的主要场所 | 信息转换 |
|---|---|---|---|---|---|
| 复制 | DNA双链 | DNA双链 | DNA聚合酶、解旋酶等 | 细胞核(真核) | DNA序列 → DNA序列 |
| 转录 | DNA模板链 | 单链RNA | RNA聚合酶 | 细胞核(真核) | DNA序列 → RNA序列 |
| 翻译 | mRNA | 多肽链/蛋白质 | 核糖体、氨酰-tRNA合成酶 | 细胞质 | RNA密码子 → 氨基酸序列 |
生物大分子
生物大分子是构成生命体并执行生命功能的巨型分子,通常由较小的有机单体通过共价键聚合而成。它们是生命的物质与功能基石,主导了细胞的结构、信息传递、能量转换和化学反应。
四大类生物大分子概览
| 大分子类别 | 基本单体(构建单元) | 连接键 | 主要聚合物形式与核心功能 |
|---|---|---|---|
| 蛋白质 | 氨基酸(20种常见) | 肽键 | 多肽链 → 蛋白质。功能的主要执行者:构成酶(催化反应)、结构蛋白、抗体、激素、受体、运输蛋白等。 |
| 核酸 | 核苷酸(含碱基、戊糖、磷酸) | 磷酸二酯键 | DNA(脱氧核糖核酸):遗传信息的存储载体,双螺旋结构。 RNA(核糖核酸):遗传信息的传递与功能执行者,单链,包括mRNA、tRNA、rRNA等。 |
| 多糖 | 单糖(如葡萄糖、果糖) | 糖苷键 | 淀粉、糖原:能量的储存形式。 纤维素、几丁质:植物和节肢动物的结构材料。 复杂多糖:细胞识别、信号传递(如细胞表面糖萼)。 |
| 脂质 | 多样性高,非严格聚合物(如脂肪酸、甘油、异戊二烯等) | 酯键等 | 脂肪(甘油三酯):高密度能量储存与保温。 磷脂:构成所有生物膜(如细胞膜)的基本骨架。 固醇类(如胆固醇):膜流动性调节、激素前体。 |
病理学基础
基础病理过程是指疾病发生时,不同器官、系统中共同存在的、典型的规律性生命活动改变。
炎症
机体对损伤因子所发生的以防御反应为主的病理过程,核心是血管反应。
基本表现:红、肿、热、痛和功能障碍。
关键环节:
- 血管反应:局部血管扩张、血流加快(炎性充血),继而血管通透性增加,血浆部分渗出。
- 白细胞渗出与吞噬:白细胞游出血管,趋化至损伤部位,吞噬和消灭病原体或坏死组织。
- 类型:
- 急性炎症:起病急,以渗出和中性粒细胞浸润为主,结局多为痊愈、迁延或转为慢性。
- 慢性炎症:病程长,以淋巴细胞、浆细胞浸润和肉芽组织增生为特征。
肿瘤
一种异常增生性疾病,其核心特征是细胞的失控性生长和分化异常。
肿瘤性增生与非肿瘤增生的根本区别:具有相对自主性(生长不受机体调控)、失去分化成熟能力(细胞幼稚、异型性)、无生理功能、浸润与转移的潜能。
关键概念:
- 异型性:肿瘤细胞在形态和组织结构上与其来源的正常组织之间的差异。异型性越大,恶性程度越高。
- 转移:恶性肿瘤细胞从原发部位侵入淋巴管、血管或体腔,迁徙到其他部位继续生长。这是恶性肿瘤最重要的生物学特征。
- 良恶性肿瘤区别:核心在于是否浸润和转移。良性肿瘤通常膨胀性生长、有包膜、不转移;恶性肿瘤则浸润性生长、无包膜、易转移。
免疫学基础
免疫学基础与生物标志物是现代医学诊断、治疗和预防的核心支柱。前者阐述了机体防御与监视的复杂系统,后者则提供了客观衡量该系统状态及疾病进程的“标尺”。
免疫系统
免疫系统的核心功能是识别”自我“与”非我“,并清除”非我“(如病原体、异常细胞),同时维持对自身组织的耐受。
1.固有免疫与适应性免疫
| 特性 | 固有免疫(非特异性免疫) | 适应性免疫(特异性免疫) |
|---|---|---|
| 反应速度 | 立即至数小时(快速) | 数天(初次反应较慢,有记忆性) |
| 特异性 | 识别病原体共有模式(如LPS),广谱 | 识别特定抗原表位,高度特异 |
| 记忆性 | 无 | 有,产生长期保护 |
| 主要组成 | 物理屏障(皮肤、黏膜)、免疫细胞(巨噬细胞、中性粒细胞、自然杀伤细胞NK)、体液因子(补体、溶菌酶) | 免疫细胞(T淋巴细胞、B淋巴细胞)、抗体 |
2.关键细胞与分子
巨噬细胞/树突状细胞:既是固有免疫的“清道夫”,也是适应性免疫的抗原呈递细胞,负责吞噬病原体并将抗原信息“展示”给T细胞。
T淋巴细胞:
- 辅助T细胞:免疫反应的“指挥官”,通过分泌细胞因子激活其他免疫细胞。
- 细胞毒性T细胞:直接识别并杀死背病毒感染的细胞或癌细胞。
B淋巴细胞:被激活后分化为浆细胞,大量产生和分泌抗体。
抗体:由B细胞产生,能特异性结合抗原,通过中和、调理吞噬等机制清除病原体。
细胞因子:免疫细胞间传递信号的蛋白质小分子,如干扰素、白细胞介素,调控免疫反应的强度与方向。
3.免疫应答的基本过程
- 识别:抗原呈递细胞捕获并处理抗原,呈递给T细胞。
- 活化与增殖:T、B细胞被特异性激活,大量克隆增殖。
- 效应:产生抗体、激活杀伤细胞等,清除抗原。
- 消退与记忆:抗原清除后,大部分效应细胞死亡,但回留下记忆性T/B细胞,实现长期免疫。
生物标志物
生物标志物是指在体液、组织或细胞中客观测量和评估,能指示正常生理过程、病理过程或对治疗干预反应的指标。
1.核心价值与用途
- 早期筛查与风险预测:如检测AFP用于肝癌高危人群筛查。
- 辅助诊断:如检测心肌肌钙蛋白诊断急性心肌梗死。
- 疾病分型与分期:如根据雌激素受体状态对乳腺癌分型。
- 预后评估:如检测某些基因表达判断癌症复发风险。
- 指导治疗(伴随诊断):如检测HER2基因扩增决定是否使用靶向药曲妥珠单抗。
- 监测疗效与复发:如监测PSA水平变化评估前列腺癌治疗效果。
2.主要类型(按分子性质)
- 蛋白质类:最广泛,如酶(ALT/AST)、激素(如胰岛素)、抗体、肿瘤标志物(CEA,CA19-9)。
- 核酸类:DNA突变、甲基化;RNA表达谱;循环肿瘤DNA等,用于基因诊断和精准医疗。
- 代谢物类:血糖、胆固醇、尿酸等,反映机体代谢状态。
- 细胞类:循环肿瘤细胞、特定免疫细胞亚群计数(如CD4+ T细胞计数用于评估艾滋病病情)。
3.理想生物标志的特征
特异性高、敏感性好、检测方法稳定可靠、采样方便(如血液)、与临床结局明确相关。
总结:免疫学揭示了身体防御与平衡的内在原理,而生物标志物则是将这一复杂原理及各种疾病状态,转化为可量化、可操作的客观指标的工具。两者结合,构成了现代精准医学的基石:通过检测特定的免疫标志物或其他生物标志物,我们不仅能诊断疾病,还能评估免疫状态、预测治疗反应,从而实现个体化的疾病管理。
生物医用材料
材料分类及其特性
一、按材料性质分类(从传统材料学角度)
| 类别 | 特点 | 典型材料举例 |
|---|---|---|
| 医用金属材料 | 高强度、高韧性、耐疲劳,但可能存在腐蚀、磨损碎屑、弹性模量不匹配(应力屏蔽)等问题。 | 不锈钢、钴基合金、钛及钛合金、镍钛形状记忆合金、可降解镁/锌合金 |
| 医用高分子材料 | 种类多、易加工、性能可调范围广。可以是惰性的、可降解的,或具有特定功能(如水凝胶)。 | 聚乙烯、聚四氟乙烯、聚酯、硅橡胶、聚氨酯、PLA/PGA、胶原、透明质酸 |
| 生物陶瓷材料 | 高硬度、高耐磨、优异的生物相容性,但通常较脆。包括惰性陶瓷、活性陶瓷和可降解陶瓷。 | 氧化铝、氧化锆(惰性);羟基磷灰石、生物活性玻璃(活性);磷酸三钙(可降解) |
| 医用复合材料 | 将两种或以上材料复合,以综合各组分的优点,克服单一材料的缺点。 | 碳纤维增强聚合物、羟基磷灰石增强聚合物、金属表面陶瓷涂层 |
二、按与生物体的相互作用分类(直接决定了材料的应用场景)
| 类别 | 核心定义与目标 | 典型材料举例 | 主要应用场景 |
|---|---|---|---|
| 生物惰性材料 | 在体内化学性质稳定,不与周围组织发生明显的化学反应或引发强烈的免疫排斥,旨在被组织“和平共存”地包裹。 | 医用不锈钢、钴铬合金、钛及钛合金、氧化铝陶瓷、超高分子量聚乙烯、医用硅橡胶 | 人工关节、骨板/骨钉、牙科种植体、心脏起搏器外壳、人工晶体 |
| 生物活性材料 | 能与周围骨组织甚至软组织形成化学键合(如骨性结合),或诱导特定的细胞反应,促进组织修复与再生。 | 生物活性玻璃、羟基磷灰石、磷酸钙陶瓷、某些复合材料 | 骨缺损填充、人工骨、骨水泥、牙科修复、涂层(改善植入体骨整合) |
| 生物可降解/吸收材料 | 在完成支撑、修复等使命后,能在体内被安全地降解、吸收或代谢,最终被新生组织替代。 | 聚乳酸、聚乙醇酸及其共聚物、胶原蛋白、壳聚糖、镁合金 | 可吸收缝合线、药物控释载体、组织工程支架、可吸收骨钉/血管支架 |
生物相容性与生物学评价
生物相容性是医用材料设计的出发点和落脚点,它超越了简单的“无毒”概念,是一个动态的、与具体应用场景深度耦合的系统性要求。
生物学评价则是保障这一要求的科学方法论和法规门槛,它通过一套标准化、分层级的测试体系,系统性地排查材料从化学毒性到长期生物安全性的各类风险。
随着材料科学与生命科学的交叉融合,对生物相容性的理解正从“避免不良反应”的被动防御,迈向“引导理想反应”的主动设计新阶段。
生物相容性
生物相容性并非单一属性,而是指材料在特定应用场景下,与人体相互作用时,引发适宜人体反应的综合能力。其核心是“平衡”--材料在发挥预期功能的同时,不应对人体产生有害作用。
1.两大核心维度
- 组织相容性:材料与组织、细胞接触时的反应。理想情况是材料不被排斥,允许细胞正常附着、增殖,不引起慢性炎症、纤维包裹过厚或细胞毒性。
- 血液相容性:材料与血液接触时的反应。关键要求包括:
- 抗血栓性:不激活凝血系统,不形成血栓。
- 抗溶血性:不破坏红细胞。
- 白细胞相容性:不引起过度的白细胞激活或炎症反应。
2.影响生物相容性的关键材料特性
- 化学因素:材料本体及可浸出物(如单体、添加剂、催化剂残留)的毒性。
- 物理因素:表面粗糙度、形状、孔隙率、亲疏水性、弹性模量等。
- 生物学因素:材料对蛋白质吸附、细胞信号传导、免疫系统识别的影响。
生物学评价
生物学评价是一个基于风险管理的系统工程,遵循“具体问题具体分析”的原则,其流程和内容由材料的性质、接触部位和接触时间决定。
1.评价的基本原则
- 风险导向:评价的深度与材料的风险等级成正比。植入物比表面接触器械要求更严苛。
- 阶段式进行:通常先进行体外试验,再进行体内试验。
- 遵循标准:主要依据ISO 10993系列(国际)和GB/T 16886系列(中国)标准。
2.生物学评价的通用步骤
- 材料表征:明确材料的化学成份、物理结构、潜在可浸提物。
- 确定器械分类:根据接触性质(表面、体外、植入)和接触时间(短期<24h、长期>30d、持久>30d)进行分类。
- 选择评价试验:基于分类,从标准推荐的试验矩阵中选择必要的测试项目。
3.核心生物学评价试验项目
| 评价类别 | 典型试验项目 | 主要目的与意义 |
|---|---|---|
| 细胞毒性 | 体外细胞培养试验(如MTT法、琼脂扩散法) | 筛选试验,评估材料浸提液对细胞生长、增殖的抑制或破坏作用,是基本的生物安全性指标。 |
| 致敏性 | 豚鼠最大化试验、局部淋巴结试验 | 评估材料或其浸提物引起机体过敏反应(如迟发型超敏反应)的潜在性。 |
| 刺激/皮内反应 | 皮肤刺激试验、皮内刺激试验 | 评估材料对皮肤或皮下组织的非特异性炎症刺激作用。 |
| 全身毒性 | 急性/亚急性/亚慢性/慢性全身毒性试验 | 评估材料浸提液通过单一或多次接触对机体全身器官和系统的有害影响。 |
| 遗传毒性 | Ames试验、染色体畸变试验、微核试验 | 评估材料是否引起基因突变、染色体损伤等遗传物质改变,是致癌性的早期筛查。 |
| 植入后局部反应 | 皮下/肌肉/骨植入试验(短期与长期) | 关键体内试验。直接观察材料植入活体组织后,引起的炎症、纤维囊形成、组织坏死等局部反应。 |
| 血液相容性 | 体外溶血试验、血栓形成试验、补体激活试验 | 专门评估材料与血液成分相互作用,是否引起溶血、凝血或免疫系统激活。 |
| 致癌性 | 长期动物植入试验(通常>1年) | 评估材料长期存在体内是否诱发肿瘤。通常仅对长期/持久接触的植入材料进行。 |
| 生殖与发育毒性 | 根据接触途径和风险决定是否需要进行 | 评估材料对生殖功能、胚胎发育的影响。 |
材料表面改性与功能化
材料表面改性与功能化是生物医用材料领域的核心工程技术。其核心理念是:在不改变材料本体优良力学性能的前提下,通过改变其最外层的物理化学性质,赋予材料全新的表面功能,从而精准调控其与生物环境的相互作用。
表面改性
一、表面改性的意义
当材料植入体内,生物环境(蛋白质、细胞、组织)首先接触并“感知”的是材料表面(几个纳米到微米的厚度)。这个初始相互作用决定了后续所有的生物反应。因此,表面是材料与生命系统对话的“界面”。
主要目标:
1.提升生物相容性:减少异物反应、抑制血栓形成、减轻炎症。
2.赋予特定生物功能:促进细胞黏附与生长(如成骨细胞)、或抑制细胞黏附(如抗菌、抗污)。
3.改善力学适配性:如增强表面润滑性(人工关节)、或调整表面硬度/模量。
4.引入治疗或监测功能:固定药物、生长因子、基因或传感器。
二、表面改性的主要方法分类
1.物理改性
通过物理手段改变表面形貌或附着新层,一般不形成强化学键。
等离子体处理:
- 原理:利用等离子体(电离气体)轰击材料表面。
- 效果:能清洁表面、引入活性集团(如:
,显著提高表面能亲水性)、获进行等离子体聚合沉积一层薄膜。这是最常用、最有效的表面活化方法之一。
离子注入与沉积:
- 原理:将高能离子(如氮、银、钙离子)注入材料表面,或在表面沉积薄膜(如类 金刚石碳膜)。
- 效果:可极大提高表面硬度、耐磨性、并赋予抗菌(银离子)或生物活性(钙离子)。
表面图案化:
- 原理:使用光刻、激光刻蚀等技术在表面制造微米/纳米级的特定拓扑结构(如沟槽、柱状阵列)。
- 效果:能直接引导细胞定向排列(接触引导),例如在神经导管内壁制造微沟槽引导神经轴突定向再生。
2.化学改性
通过化学反应在表面接枝或构建新的分子层。
化学接枝:
- 原理:通过表面预先引入的活性基团,共价连接上功能分子链(如聚乙二醇PEG、肝素、多肽RGD)。
- 效果:功能强大且稳定。例如,接枝PEG可形成“分子刷”产生空间排斥,有效抗蛋白质吸附和细胞粘附(抗污表面);接枝肝素可抗凝血;接枝RGD多肽可特异性促进细胞粘附。
自组装单分子层:
- 原理:特定分子(如烷基硫醇在金表面)通过头基自发、紧密地排列在基底上,形成高度有序的单分子层。
- 效果:可精确控制表面的化学端基(如
疏水, 亲水),是研究表面化学对蛋白质、细胞行为影响的理想模型,也可用于构建生物传感器。
3.生物化学改性
将具有生物活性的分子固定在材料表面。
- 原理:通过物理吸附或化学偶联,将蛋白质(如胶原、纤连蛋白)、多肽、多糖(如透明质酸)、生长因子或DNA固定在表面。
- 效果:使材料表面“生物化”,主动向周围组织发出特定信号。例如,在钛种植体表面固定骨形态发生蛋白,可强力诱导骨整合。
功能化
1.抗凝血/血液相容性表面:
- 策略:接枝肝素(天然抗凝剂);接枝水凝胶或PEG(形成水合层,减少蛋白质和血小板吸附);表面内皮化(促进内皮细胞在血管支架表面生长,形成天然屏障)。
2.抗菌表面:
- 策略:接触杀菌型(如接枝季铵盐、抗菌肽);释放杀菌型(负载并缓释银离子、抗生素);抗粘附型(超亲水或超疏水表面,阻止细菌初始粘附)。
3.促细胞粘附与组织整合表面:
- 策略:涂层或接枝细胞外基质蛋白(胶原、层粘连蛋白);接枝特异性多肽(如RGD序列,介导细胞整合素识别);构建多孔或粗糙的形貌(利于骨组织长入)。
4.抗污(抗非特异性蛋白吸附)表面:
- 策略:接枝两性离子聚合物(如聚磺基甜菜碱)或PEG,形成紧密的水合层,形成能量屏障阻止蛋白质变性吸附。这是许多高性能植入体和生物传感器的基石。
5.药物/基因递送表面:
- 策略:通过涂层、微球或化学键合,在表面负载治疗剂,实现局部、可控的释放。例如,在心血管支架表面涂覆抗增殖药物(雷帕霉素),防止血管再狭窄。
纳米材料
纳米材料在生物医学中的应用是当今前沿交叉领域的核心,它通过利用纳米尺度(通常1-100纳米)下的独特物理化学性质,为解决传统医学的诸多难题提供了革命性工具。其核心优势在于尺度与生命基本单元(如蛋白质、DNA、细胞器)相匹配,从而能进行高效、精准的相互作用。
一、纳米材料的独特性质
1.尺寸效应:与细胞、病毒、蛋白质尺寸相近,易于穿越生物屏障(如血管壁、血脑屏障),并被细胞内吞。
2.超大比表面积:可负载大量药物、基因或显影剂,实现高效载带与递送。
3.表面易功能化:表面可修饰靶向分子(如抗体、多肽)、聚合物(如PEG增加隐形性)或环境响应基团,实现智能化。
4.特殊光学/磁学性质:如金纳米棒的表面等离子共振、量子点的荧光、超顺磁氧化铁纳米粒的磁响应,适用于成像与治疗。
二、主要应用领域
1.药物与基因递送
这是最成熟的应用领域,旨在解决传统给药方式的痛点。
- 靶向递送:在纳米颗粒表面连接靶向配体(如抗体、叶酸),使其能主动识别并富集在病变组织(如肿瘤),提高疗效,降低全身副作用。
- 控释和缓释:利用对特定刺激(肿瘤微环境的低pH、特定酶、近红外光)响应的纳米材料包裹药物,实现药物在病灶部位的精准、可控释放。
- 突破生物屏障:设计特殊纳米载体,帮助药物穿越血脑屏障,治疗脑部疾病;或通过黏膜递送,提高生物利用度。
- 基因治疗载体:阳离子聚合物或脂质纳米粒可有效压缩并保护DNA/RNA,将其递送入细胞,用于基因沉默(如siRNA)、基因编辑(如CRISPR-Cas9系统)或mRNA疫苗(如新冠疫苗的核心技术)。
2.诊断与生物成像
利用纳米材料作用高灵敏、多模态的成像对比剂或检测标签。
体外诊断:
- 侧流层析试纸条:使用金纳米颗粒作为显色标签,实现快速检测(如早孕、传染病)。
- 生物传感器:基于纳米材料(如石墨烯、碳纳米管)的高导电性和大比表面积,可高灵敏检测疾病标志物。
体内成像:
- 磁共振成像:超顺磁氧化铁纳米粒作为T2造影剂,增强肿瘤等病变组织的对比。
- 荧光成像:量子点、上转换纳米粒子具有亮度高、稳定性好、可调发射波长等优点,用于细胞标记和肿瘤示踪。
- 光声成像:金纳米棒、碳纳米管等可将吸收的光能转化为声波,提供高分辨率深层组织成像。
- 多模态成像:将不同功能的纳米材料集成于一体,实现“一次组设,多种模式成像”,获取互补信息。
3.治疗学--“诊疗一体化”
将诊断与治疗功能整合于单一纳米平台,实现“看到哪里,打到哪里”。
- 光热治疗:金纳米壳、石墨烯等能高效吸收近红外光并转化为热能,局部加热杀死肿瘤细胞。
- 光动力治疗:纳米载体负载光敏剂,在特定光照下产生活性氧,杀伤靶细胞。
- 磁热治疗:交变磁场下,磁性纳米颗粒产热杀伤肿瘤。
- 协同治疗:纳米载体可同时负载化疗药、光热剂、基因药物等,实现“化疗+热疗+基因治疗”等多模式协同,克服耐药性。
4.再生医学与组织工程
- 纳米纤维支架:模拟细胞外基质的纳米纤维结构(如静电纺丝制备的纳米纤维),为细胞生长、迁移提供理想的物理引导和力学支撑。
- 生物活性纳米材料:纳米羟基磷灰石、生物活性玻璃纳米粒子可促进骨组织再生。
- 干细胞调控:纳米拓扑结构(图案、粗糙度)和表面化学可定向调控干细胞的粘附、增殖和分化。
5.抗菌应用
- 直接接触杀菌:银纳米粒子、氧化锌纳米粒子等能破环细胞细胞膜,产生活性氧,有效对抗耐药菌。
- 光催化/光热抗菌:二氧化钛纳米粒子在光照下催化产生活性氧;纳米光热材料可局部升温杀灭细菌和生物膜。
生物医学传感器与医用仪器
传感器基本原理与分类
传感器是将外界非电信号(物理、化学、生物量)按一定规律转换为可用电信号(电压、电流、电阻等)的装置或器件,是实现自动检测与控制的首要环节。
一、传感器的基本原理
其核心工作流程可概括为“感知-转换-输出”:
1.感知:通过敏感元件直接感受被测量(如温度、压力、光照、浓度)。
2.转换:利用转换元件的物理、化学或生物效应,将感知的非电量转换为电参量(如电阻、电容、电荷)的变化。这是传感器的核心。
3.信号调理与输出:通过内置或外接电路,将变化的电参量处理成标准、易于传输和处理的电信号(如4-20mA电流、0-5V电呀、数字信号)。
二、传感器的分类
按输入被测量(检测对象)分类。
| 大类 | 主要被测量举例 | 典型传感器实例 |
|---|---|---|
| 物理量传感器 | 力、压力、位移、速度、加速度、流量、温度、湿度、光强、声音、磁场等。 | 应变片(力)、热电偶(温度)、光敏电阻(光强)、麦克风(声音)、加速度计(加速度)。 |
| 化学量传感器 | 气体成分、液体离子浓度(pH)、湿度、特定化学物质(如葡萄糖、酒精)浓度等。 | 氧气传感器、pH电极、酒精检测仪、一氧化碳报警器。 |
| 生物量传感器 | 酶、抗原/抗体、DNA、微生物、细胞活性等生物分子或生命活动参数。 | 血糖试纸(酶电极)、妊娠试纸(免疫层析)、DNA生物芯片、微生物电极。 |
生理参数测量技术
血压
血压指血液对单位面积血管壁产生的侧压力,通常以毫米汞柱为单位。
1.测量原理与技术分类
有创血压测量(金标准)
- 原理:将充满生理盐水的导管经动脉穿刺,直接置入待测血管腔内,导管另一端连接外部压力传感器。血管内的压力通过导管内液体传导至传感器,转换为电信号。
- 特点:**连续、实时、精确。**能获得动脉压力波形,计算收缩压、舒张压和平均动脉压。
- 应用:主要用于重症监护室、手术室等对血压监测要求极高的场合。
无创血压测量(主流方法)
- 原理:通过袖带在肢体外加压,阻断并恢复动脉血流,间接推算血压。主要有两种方法:
听诊法(柯氏音法):
- 过程:袖带充气压迫肱动脉至血流完全阻断,然后缓慢放气。医生用听诊器在袖带下游的动脉处监听。当听到第一声搏动音(柯氏音第I时相)时,对应的袖带压力为收缩压;当搏动音突然变弱或消失(柯氏音第V时相)时,对应的压力为舒张压。
特点:传统标准方法,依赖操作者,无法连续测量。
示波法(电子血压计原理):
- 过程:袖带充放气过程中,检测由动脉搏动引起的袖带内压力震荡波。震荡波幅度会随袖带压力变化,其幅度突然增大时对应的压力近似于平均动脉压,再通过算法推算出收缩压和舒张压。
- 特点:自动化、易操作,是家用和多数临床电子血压计的基础。准确性受算法、袖带尺寸和佩戴位置影响。
连续无创血压监测:
- 原理:容积钳法。在手指上使用可动态调节压力的指套,通过光电传感器(PPG)监测血流容积,实时调节指套压力以保持血管容积恒定,该调节压力即连续动脉血压。
- 设备:如Finapres、ClearSight(一种连续无创血流动力学监测系统)。
- 特点:可提供接近有创测量的连续血压波形,用于术中或ICU动态监测。
- 原理:通过袖带在肢体外加压,阻断并恢复动脉血流,间接推算血压。主要有两种方法:
心电测量
心电记录的是心脏周期性电激动在体表产生的电位变化。
1.基本原理
- 电生理基础:心脏窦房结自发产生电脉冲,经特殊传导系统(房室结、希氏束、蒲肯野纤维)有序传播,引发心肌细胞除极与复极。这一宏观电流在身体这个容积导体中形成电场,可在体表测得。
- 心电图波形:一个标准心搏周期(P-QRS-T):
- P波:心房除极。
- QRS波群:心室除极(主要电活动,波幅最高)。
- T波:心室复极。
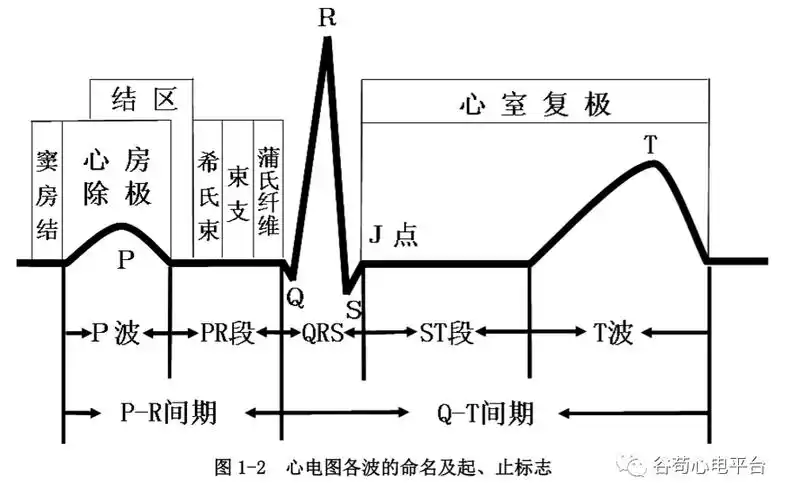
2.测量技术
- 导联系统:通过放置在体表特定位置的电机组合来“观察”心脏电活动。
- 标准12导联:包括肢体导联(I,II,III,aVR,aVF)和胸导联(V1-V6)。提供心脏在额面和水平面的多角度“视图”,用于全面临床诊断。
- 单导联/少导联:简化配置(如双手持、胸贴片),主要用于心率监测、心律失常筛查(如房颤)和可穿戴设备。
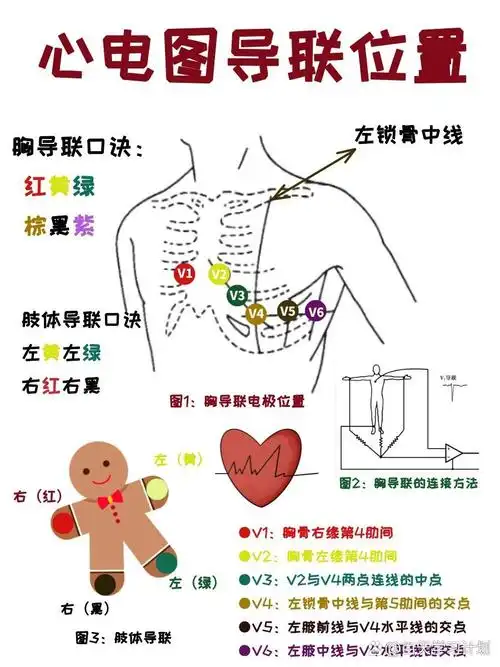
- 设备类型:
- 静态心电图机:在医院短时间内记录12导联心电图,用于诊断心肌梗死、心律失常、传导阻滞等。
- 动态心电图:便携设备(Holter)连续记录24-72小时心电活动,用于捕捉间歇性症状(如偶发心悸、晕厥)相关的心率失常。
- 心电监护仪:实时显示1-3个导联的心电波形和心率,用于手术、急诊和病房的持续监测。
- 可穿戴心电设备:智能手表、胸贴等,提供单导联心电记录和自动分析(如房颤提示),用于日常健康管理和筛查。
血氧
血氧饱和度指血液中氧合血红蛋白占全部可结合血红蛋白的百分比。
1.测量原理:光电容积脉搏波法
- 光吸收特性差异: 氧合血红蛋白和还原血红蛋白对特定波长的光吸收率不同。
- 氧合血红蛋白更多吸收红外光。
- 还原血红蛋白更多吸收红光。
- 搏动性血流信号:动脉血随心跳搏动,血管容积周期性变化;而静脉血、皮肤、骨骼等组织对光的吸收是恒定不变的。
2.测量过程与设备
- 设备:最常见的是指夹式脉搏血氧仪。
- 过程:传感器一侧发射红光和红外光,穿过手指(或耳垂等部位)后,另一侧的光电探测器接收透射光强度。
- 计算:仪器通过分析两种光在搏动期间的吸收变化比值,利用预先标定的经验公式,即可计算出动脉血氧饱和度。
- 输出:显示
(外周血氧饱和度)数值和脉搏波形/心率。
体温
体温是机体核心温度的表征,反映产热与散热的平衡。
1.测量原理与分类
主要分为接触式和非接触式。
接触式测量
- 原理:基于热平衡,使感温元件与测量部位充分接触,达到热平衡后读数。
- 主要方法与部位:
- 水银/酒精温度计:利用液体热胀冷缩,测量腋下、口腔、直肠温度。直肠温度最接近核心温度。
- 电子温度计(热敏电阻):利用半导体电阻随温度变化的特性,测量部位同上,更安全快捷。
- 耳温枪(热电堆):测量鼓膜释放的红外辐射能量。鼓膜温度被认为能快速反映核心温度变化。
非接触式测量
- 原理:红外辐射测温法。所有物体都向外辐射红外线。
- 设备:额温枪、红外热成像仪。
- 过程:传感器接收人体额头或颞动脉区域皮肤散发的红外辐射,转换为电信号并换算成温度显示。
- 特点:快速、无接触、适合筛查。但测量结果易受环境温度、出汗、测量距离和角度影响,通常精度低于接触式方法,且测量的是体表温度。
体外诊断技术与即时检测设备
体外诊断技术与即时检测设备是现代医疗体系的“侦察兵”,它们通过在人体外对血液、体液、组织等样本进行分析,为疾病的预防、诊断、治疗监测和预后评估提供关键依据。其中即时检测是体外诊断领域发展最快、最具变革性的分支。
体外诊断技术
一、概念
指人体之外,通过对样本进行检测来获取临床诊断信息的所有技术手段。它是实验室医学的核心,涵盖了从大型自动化分析仪到小型手持设备的广阔范围。
二、技术分类
| 技术分类 | 基本原理 | 主要检测项目 | 典型设备 |
|---|---|---|---|
| 生化诊断 | 利用样本中待测物质与试剂发生特异性化学反应,通过吸光度、浊度等变化进行定量分析。 | 血糖、血脂、肝功能、肾功能、电解质等。 | 全自动生化分析仪。 |
| 免疫诊断 | 利用抗原-抗体特异性结合反应进行检测,标记物包括酶、荧光、化学发光物质等。 | 传染病标志物(如乙肝、HIV)、肿瘤标志物、激素、心肌标志物(如肌钙蛋白)等。 | 酶联免疫吸附试验仪、化学发光免疫分析仪、荧光免疫分析仪。 |
| 分子诊断 | 在分子水平(DNA、RNA)上,通过扩增(如PCR)和杂交等技术检测基因序列。 | 病原体核酸(如新冠病毒)、遗传病基因、肿瘤基因突变、药物代谢基因等。 | 聚合酶链式反应仪、基因测序仪。 |
| 微生物诊断 | 对病原微生物进行培养、鉴定和药敏试验。 | 细菌、真菌鉴定及抗生素敏感性。 | 血培养仪、微生物鉴定药敏系统。 |
| 血液诊断 | 对血液中有形成分(细胞)和凝血功能进行分析。 | 血常规、凝血四项等。 | 全自动血细胞分析仪、凝血分析仪。 |
| POCT | 并非独立技术,而是将上述技术(尤其是生化、免疫)集成化、微型化,实现快速现场检测。 | 覆盖感染性疾病、心血管疾病、糖尿病、妊娠检测等多领域。 | 血糖仪、免疫层析试纸条(如早孕试纸)、手持式血气分析仪、小型荧光免疫分析仪。 |
即时检测设备
1.概念
即时检测,又称床旁检测,是IVD的一个重要细分领域。POCT强调“即时、即地、即操作者”三大要素:
- 即时:快速获取结果(通常在采样后数分钟至20分钟内)。
- 即地:在患者身边或采样现场进行,无需将样本送往中心实验室。
- 即操作者:操作简便,经过简单培训的非检验专业人员(甚至患者本人)即可操作。
POCT是一种检测理念和应用模式,它可以搭载生化、免疫、分子等多种IVD技术平台,实现检测的“小型化、便携化、快速化”。
2.主流POCT技术原理
- 干化学技术:将多种反应试剂干燥固定在纸片或多层薄膜上,加入液态样本(如血液、尿液)后,样本作为反应介质,与干试剂发生显色反应,通过肉眼观察(定性)获仪器判读(半定量/定量)结果。例如:尿液试纸条、干式生化分析仪。
- 免疫层析技术(胶体金法):这是最广为人知POCT技术。将标记了交替金(呈红色)的抗体固定在试纸条上,样本在毛细作用下向前层析。若样本中含有目标抗原,会与金标抗体结合,并在检测线被捕获,形成红色条带,实现定性获半定量检测。例如早孕试纸、新冠抗原检测试纸。
- 免疫荧光技术:使用荧光物质(而非胶体金)作为标记物。样本中的目标物与荧光标记抗体结合后,在检测区被捕获,通过专用荧光读数仪检测荧光强度,实现高灵敏度的定量检测。这是目前中高端POCT的主流技术之一,广泛应用于心肌标志物、炎症指标(如PCT、CRP)的定量检测。
- 生物传感器技术:将生物识别元件(如酶、抗体、核酸)与物理化学换能器(如电极、光纤)结合,将生物反应转化为可测量的电信号或光信号。例如:血糖仪(葡萄糖氧化酶电极)、手持式血气电解质分析仪(离子选择性电极)。
- 微流控与生物芯片技术:在芯片上构建微米尺度的管道和反应室,实现样本的进样、分离、反应、检测全流程集成化和自动化,是“芯片实验室”的体现。数字微流控技术能通过电场精确操控纳升-微升级液滴,实现高度自动化的多重检测,是前沿方向。
医疗仪器系统
根据医疗仪器系统在临床流程中的核心作用,主要可分为诊断设备、治疗设备和监护设备三大类。它们贯穿于疾病预防、诊断、治疗和康复的全过程,共同构成了完整的临床诊疗闭环。
诊断设备
核心功能:用于探查、识别和评估疾病或生理状态,为临床决策提供客观依据,辅助医生确诊。
主要分类
影像诊断设备
通过物理手段生成人体内部结构的图像。
X射线设备:利用X射线的穿透行和组织吸收差异成像。包括普通X光机(用于骨骼、胸部)、数字减影血管造影机(DSA,用于血管介入)、计算机断层扫描(CT,提供横断面三位信息,速度快,用于急诊、肿瘤等)。
磁共振成像:利用强磁场和射频脉冲,探测人体内氢原子核的磁共振信号,重建出高软组织对比度的图像。无辐射,对神经系统、关节、软组织病变显示极佳。
超声诊断设备:利用超声波在组织界面的反射成像。实时、无创、无辐射,广泛应用于产科、心脏(超声心动图)、腹部、浅表器官及血管检查。多普勒技术可评估血流速度与方向。
核医学设备:向体内引入微量放射性核素标记的药物(示踪剂),通过设备探测其分布。如单光子发射计算机断层成像(SPECT)和正电子发射断层成像(PET),反映的是功能和代谢信息,常用于肿瘤早期发现、心肌存活评估等。PET-CT/MRI实现了功能与解剖图像的精准融合。
实验室诊断设备
对离体样本(血、尿、组织等)进行定性和定量分析。
临床化学分析仪:自动化检测血糖、血脂、肝肾功能、电解质等生化指标。
免疫分析仪:利用抗原-抗体反映,高灵敏度检测激素、肿瘤标志物、传染病病原体抗体/抗原等。化学发光法是当前主流高端技术。
血液分析仪:全自动完成血细胞计数、分类和形态学初步分析。
微生物鉴定与药敏系统:快速鉴定病原菌并测试抗生素敏感性,知道抗感染治疗。
分子诊断设备:如PCR仪、基因测序仪,在核酸水平进行检测,用于病原体核酸、遗传病、肿瘤基因分型等,是精准医学的基础。
功能检查设备
评估特定器官或系统的生理功能。
心电图机:记录心脏电活动,诊断心率失常、心肌缺血/梗死等。
脑电图机:记录大脑电活动,用于癫痫、睡眠障碍、脑功能评估。
肺功能仪:测量肺容量和通气功能,诊断慢性阻塞性肺疾病、哮喘等。
内窥镜系统:通过光学镜头直接观察空腔脏器内部(如胃镜、肠镜、支气管镜),并可进行活检和治疗。
治疗设备
治疗设备的核心任务是“干预与纠正”,即利用物理、化学或机械手段消除病灶、修复功能或缓解症状。
手术设备
传统手术器械:手术刀、剪、钳、拉钩等。
能量外科设备:利用能量进行切割、凝固、止血。
- 高频电刀:最常用,利用高频电流产生热效应。
- 超声刀:利用超声波振动产生摩擦热和空化效应,切割精确,烟雾少。
- 激光手术设备:利用激光能量汽化或切除组织,用于眼科、整形、泌尿外科等。
微创/内镜手术设备:包括腹腔镜、胸腔镜及配套的摄像、光源、气腹机和各种长柄操作器械,实现小切口手术。
手术机器人系统:如达芬奇手术系统,提供三位高清视野、滤除收不震颤、可进行精细操作,是高端微创手术的代表。
放射治疗设备
利用放射线(如X射线、
直线加速器:最主流的放疗设备,可产生高能X射线和电子线,常与调强适形放疗(IMRT)、图像引导放疗(IGRT)和容积旋转调强放疗(VMAT)技术结合,实现高精度追老。
伽马刀/射波刀:属于立体定向放射外科,通过多束射线高精度聚焦于颅内或体部小病灶,单次或少数几次给予高剂量,用于治疗脑动静脉畸形、脑转移瘤等。
相关应用:大物是也:re天使也有实习期质子/重离子治疗系统:利用其“布拉格峰”物理特性,使能量主要沉积在肿瘤靶区,对前方正常组织损伤极小,是当前最先进的放疗技术之一,但设备极其昂贵。
物理治疗设备
利用物理因子(声、光、电、磁、热、力)进行治疗。
体外冲击波治疗仪:用于碎石(泌尿系、胆道)及治疗骨肌疾病(如钙化性肌腱炎)。
康复设备:包括低频/中频电疗仪、磁疗仪、红外/紫外光疗仪、牵引床、各类运动训练器械等,用于功能恢复。
监护设备
监护设备的核心任务是“持续观察与预警”,即实时、连续地监测患者的生命体征和关键参数,及时发现病情变化,保障治疗安全。
生命体征监护仪
重症监护室、手术室、急诊科的标配,通常多参数集成。
监测参数:心电、血压、血氧饱和度、呼吸、体温。高端监护仪还可集成呼吸末二氧化碳、有创血流动力学(如心输出量)、脑电双频指数(用于麻醉深度监测)等。
核心功能:实时波形与数字显示、参数报警(可设置上下限)、趋势回顾、数据存储与传输。
专项监护设备
胎儿监护仪:监测产前和产程中胎心率和宫缩压力。
动态心电图/血压记录仪:患者佩戴24小时或更长时间,记录日常状态下的心电或血压变化,捕捉阵发性异常。
睡眠呼吸监护仪:用于诊断睡眠呼吸暂停综合症。
颅内压监护仪:直接或间接监测颅脑损伤或术后患者的颅内压力。
遥测监护与可穿戴设备
院内遥测监护:患者佩戴无线发射器,可在病房一定范围内自由活动,生命体征数据被中央站持续接收。
可穿戴家用监护设备:如智能手表(监测心率、血氧、心电图)、连续血糖监测仪等,用于慢性病管理和早期预警。
医疗电子
一个典型的医疗嵌入式系统硬件/软件架构如下:
| 层级 | 组成部分 | 在医疗设备中的功能与示例 |
|---|---|---|
| 硬件层 | 微控制器/微处理器 | 系统“大脑”。MCU(如ARM Cortex-M系列)集成CPU、内存、外设,适用于便携设备(血糖仪、监护仪)。MPU(如Cortex-A系列)性能更强,运行复杂OS,适用于高端设备(超声诊断仪)。 |
| 传感器与信号调理电路 | 系统“感官”。将生理信号(心电、血压、血氧)转换为电信号,并进行放大、滤波、模数转换。 | |
| 存储器 | 存储程序代码、患者数据、波形记录。包括Flash(存储程序)、RAM(运行内存)、SD卡/EEPROM(存储数据)。 | |
| 输入/输出设备 | 输入:按键、触摸屏、语音接口。 输出:LCD/OLED显示屏、打印机、声音/光报警器、电机/泵(用于治疗设备)。 | |
| 通信接口 | 实现设备互联与数据上传。有线(USB、以太网)、无线(蓝牙、Wi-Fi、ZigBee、NB-IoT)。 | |
| 软件层 | 实时操作系统 | 系统“管家”。管理任务调度、内存、外设,确保关键任务(如心电R波检测)在规定时间内完成。常见RTOS:FreeRTOS、ThreadX、VxWorks。 |
| 设备驱动程序 | 硬件与OS/应用程序间的“翻译官”,控制具体硬件(如ADC、显示屏、通信模块)的操作。 | |
| 应用程序 | 实现设备核心医疗逻辑的软件,如心电算法分析、药物剂量计算、图像重建与后处理。 |
医学影像技术
影像技术物理基础
医学影像是现代医疗的“眼睛”,它通过物理手段非侵入性地获取人体内部结构与功能信息。
其核心在于利用不同物理信号与人体组织的相互作用差异来生成图像。下
四种核心相互作用机制
医学影像技术主要建立在四种物理效应之上,每种效应对应一类主流成像模态。
| 成像模态 | 核心物理信号/源 | 与组织的相互作用基础 | 所反映的信息 |
|---|---|---|---|
| X射线/CT成像 | X射线(高频电磁波) | 衰减:光电效应、康普顿散射。不同组织(如骨骼、软组织、脂肪)对X射线的线性衰减系数不同。 | 电子密度与原子序数。主要显示解剖结构,尤其是高密度组织(骨骼、钙化)。CT通过多角度投影重建出横断面图像。 |
| 磁共振成像 | 射频脉冲与静磁场 | 核磁共振:人体内丰富的氢原子核(质子)在强磁场中发生能级分裂,接收特定频率的射频脉冲后发生共振并吸收能量,脉冲停止后释放能量(发出MR信号)。弛豫:信号衰减过程,包括T1弛豫(自旋-晶格)和T2弛豫(自旋-自旋)。 | 质子密度、弛豫时间(T1, T2)。对软组织分辨率极高,能清晰区分脑灰质/白质、肌肉、韧带、肿瘤等,并能进行功能成像(fMRI)和代谢成像(MRS)。 |
| 超声成像 | 高频超声波(机械波) | 反射(回声)与散射:超声波在遇到不同声阻抗的组织界面时发生反射。声阻抗差异越大,反射越强。多普勒效应用于测量血流速度。 | 组织声阻抗差异与运动。实时、动态显示器官形态与运动(如心脏瓣膜、胎儿),并能评估血流方向与速度。 |
| 核医学成像 | 放射性核素(示踪剂) | 放射性衰变与探测:将标记了放射性核素(如锝-99m、氟-18)的药物引入体内,其在体内特定部位(如代谢活跃的肿瘤)浓聚并发射γ光子。探测器在体外接收这些光子。 | 生物化学与功能代谢。显示示踪剂在体内的分布,反映生理功能(如葡萄糖代谢、血流灌注),常用于早期发现肿瘤、评估心肌活力。 |
小结:X射线/CT基于密度差异,MRI基于质子磁环境,超声基于声学特性,核医学基于生物化学过程。前三者主要提供解剖形态信息,而核医学及其与CT/MRI的融合(PET-CT, SPECT-CT)则提供了独特的功能代谢视角。
系统构成
1.信号产生/激发单元
- 作用:产生能与人体发生相互作用的物理信号。
- 示例:
- X射线机:X射线管(阴极灯丝、阳极靶、高压发生器)。
- MRI:超导主磁体、梯度线圈、射频发射线圈。
- 超声:超声探头中的压电晶片(电信号 -> 超声波)。
- 核医学:回旋加速器(生产发射性核素)、放射性药物合成模块。
2.信号探测与采集单元。
- 作用:接收、探测从人体出来的携带信息的信号,并将其转换为电信号。
- 示例:
- X射线/CT:平板探测器(将X光直接转换为数字信号)或影像增强器+CCD。
- MRI:射频接收线圈(接收氢原子释放的MR信号)。
- 超声:同探头压电晶片(接收回声并转换为电信号)。
- 核医学(SPECT/PET):
相机或闪烁探测器(碘化钠晶体+光电倍增管)。
3.信号处理与重建单元
- 作用:对采集到的原始电信号进行放大、滤波、数字化等处理,并运用数学算法重建出图像。
- 核心:这是系统的“计算大脑”。
- CT:使用滤波反投影或迭代重建算法,将数百个角度的投影数据重建成横断面图像。
- MRI:对接收到的K空间数据进行傅立叶变换,得到空间图像。
- 超声:对回声信号进行波束合成、对数压缩等处理,形成B-mode(亮度模式)图像。
- 核医学:通过反投影或迭代算法重建示踪剂的三维分布图。
4.图像后处理、显示与存储单元
- 作用:优化图像视觉效果,供医生判读和存档。
- 功能:窗宽窗位调节、三位重建、多平面重组、图像融合、测量分析等。
- 硬件:高性能图形工作站、专业医用显示器(高亮度、高对比度)、PACS(图像归档与通信系统)。
5.控制系统与患者支撑单元
- 作用:协调各子系统工作,保障患者安全与扫描精度。
- 包括:计算机控制系统、扫描床(精准定位与移动)、激光定位灯、生理信号门控(如心电门控用于心脏MRI/CT)、安全联锁装置(如辐射防护、急停开关)。
X射线与CT影像
X射线与CT影像是现代医学影像的基石,它们都利用X射线进行成像,但原理有本质区别:X射线得到的是三维结构的二维重叠投影,而CT获得的是人体横断面的三维断层图像。
生物医学信号处理
生物医学信号特征与预处理
生物医学信号是生命活动产生的物理或化学变化,其处理是医疗设备实现诊断、监护功能的核心环节。由于信号极其微弱且混杂大量干扰,预处理是提取有效信息的必要前提。
其核心逻辑是:**针对生物信号的固有特征,采用相应技术“去伪存真”。
特征
1.弱信号性:幅度非常小。
- 心电ECG:0.5-5mV
- 脑电EEG:10-100
V - 肌电EMG:0.1-5mV
- 这要求前端放大器必须具备高增益、低噪声的特性。
2.强噪声与干扰背景:信号被多种噪声淹没。
- 工频干扰:50/60Hz及其谐波,来自电源,幅度常大于信号本身。
- 基线漂移:低于0.5Hz的缓慢变化,由呼吸、电极接触不良等引起。
- 肌电干扰:肌肉收缩产生的高频(几十至几百Hz)随机噪声。
- 电极接触噪声:阻抗变化引起的瞬态伪迹。
- 其他生理干扰:如心电混入脑电(心电伪迹)。
3.非平稳性与随机性:
- 信号的统计特性(均值、方差、频率)随时间变化,与生理状态相关(如睡眠各期脑电波不同)。
- 存在个体差异和日间差异。
4.非线性与复杂性:
- 各生理系统相互作用,信号多由非线性机制产生,蕴含丰富动态信息。
预处理
预处理是信号分析的先决步骤,目标是抑制噪声、消除伪影、增强信号质量,为特征提取和临床诊断提供可靠数据基础。
1.典型噪声/伪影及其抑制方法
- 工频干扰:使用50/60Hz陷波器。(在心电图中,常用来消除电源干扰,增强信号清晰度)但可能损伤同频段的生理信号成分。陷波器介绍
- 基线漂移:由呼吸、电极滑动或皮肤-电极界面阻抗变化引起的低频缓慢搏动(通常<0.5Hz)。常用高通滤波或多项式拟合进行基线校正来消除。
- 肌电干扰:肌肉收缩产生的高频宽带随机噪声。可通过低通滤波(根据信号有效频带上限设定截止频率)或小波阈值去噪等方法抑制。
- 运动伪影:身体运动导致信号幅值发生阶跃性或缓慢漂移。可采用自适应滤波或盲源分离(如独立分量分析ICA)技术处理。
2.核心预处理技术
滤波:最基础且重要的去噪手段。
- 低通滤波:去除高频噪声(如肌电干扰)。
- 高通滤波:去除低频基线漂移。
- 带通滤波:仅保留信号的主要有效频带(如处理ECG常用0.5-100Hz带通滤波器)。
- 自适应滤波:能根据信号特性动态调整参数,适用于处理非平稳信号。
